1 – Especificação do produto Kyleena®

Kyleena®: sistema intrauterino de levonorgestrel em baixa dose de 5 anos (SIU-LNG)
Kyleena® é um sistema intrauterino (SIU) recentemente aprovado, contendo 19,5 mg de levonorgestrel (LNG), indicado para contracepção por até 5 anos 1.
• Independentemente da idade e paridade, Kyleena® oferece uma contracepção altamente eficaz por até cinco anos.
• Independentemente da dose diária, Kyleena® fornece uma contracepção confiável.3
• Kyleena® possui a menor estrutura em T e o tubo de inserção mais estreito disponível para um SIU.4
• Kyleena® libera a menor dose diária de LNG entre os SIUs projetados para contracepção por até 5 anos.1,5
• Quando o Kyleena® é removido, as mulheres retornam ao seu nível de fertilidade normal.
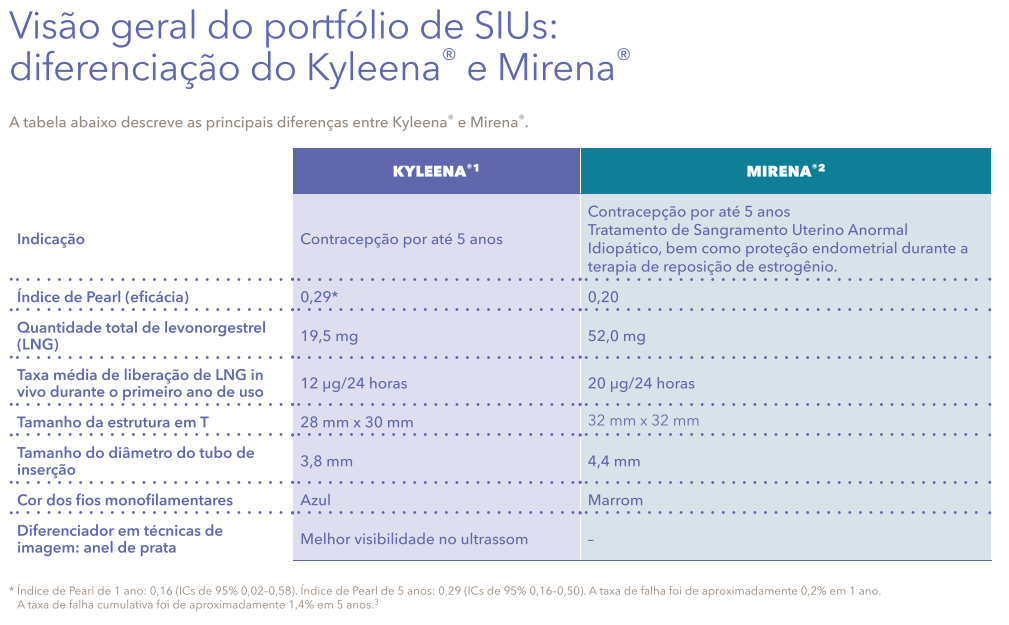
Aparência física do Kyleena® e Mirena®
A haste da estrutura de Kyleena® contém um anel de prata para identificação por ultrassom e as dimensões são menores em comparação com o Mirena®.
Os fios de remoção de cor azul estão presos ao laço no final da haste.
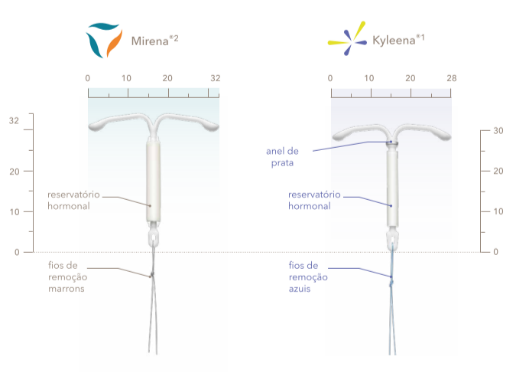
Dimensões do insertor do Mirena® e do Kyleena®
A menor dose hormonal de Kyleena® permite um menor reservatório e um tubo de inserção e menor diâmetro.
Mecanismo de ação do Kyleena®1-3
• Kyleena® é inserido na cavidade uterina e é eficaz por até 5 anos.1 • Quando colocado, o NG é liberado continuamente na cavidade uterina.
• A eficácia contraceptiva é independente da adesão da usuária.
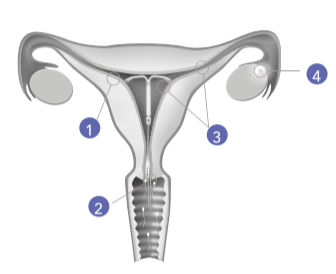
1 – O endométrio torna-se relativamente insensível ao estradiol circulante e um forte efeito antiproliferativo é observado. Modificações morfológicas do endométrio e uma fraca reação a corpo estranho local são observadas durante o uso.
2 – O muco cervical fica mais espesso e impede a passagem do espermatozoide através do canal cervical.
3 – O ambiente local do útero e das tubas uterinas inibe a mobilidade e a função espermática, impedindo a fertilização.
4 – Evidência de ovulação foi observada em quase todas as mulheres.
2 – Evidências Clínicas
Kyleena® foi estudado em mulheres nulíparas e com paridade, em dois estudos clínicos globais
As evidências do Kyleena® são baseadas em dados de 1.697 mulheres com idade entre 18 e 41 anos em dois estudos clínicos globais.


3 Inserção
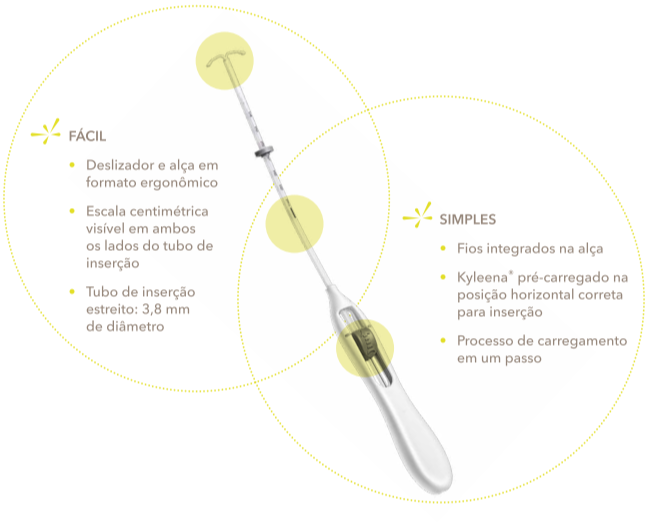
Bayer EvoInserter® permite uma inserção simples com apenas uma mão.
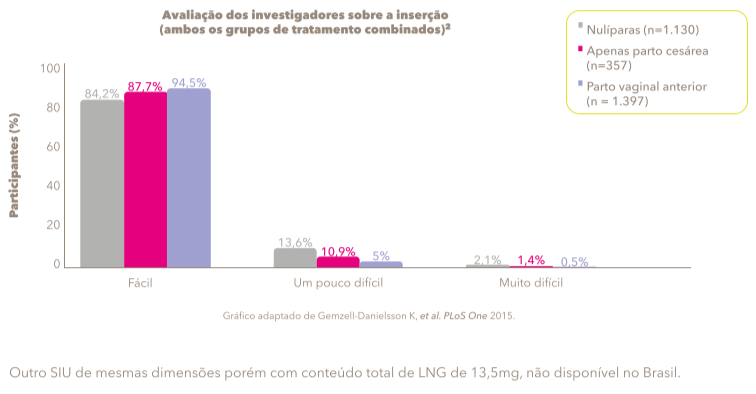
Avaliação dos investigadores sobre a inserção no estudo de Fase III1
Entre 2.884 participantes no conjunto de análise completo, 39,2% eram nulíparas e 51,5% nunca tiveram parto vaginal.
As colocações foram geralmente mais fáceis do ponto de vista do investigador em mulheres que tiveram anteriormente um parto vaginal do que em mulheres nulíparas ou mulheres com paridade que passaram apenas por cesariana (sem partos vaginais) (p <0,0001 para a diferença global).
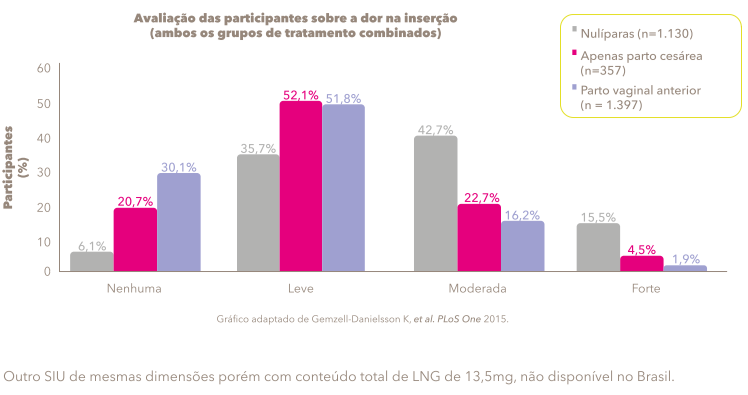
Perspectiva das mulheres sobre a inserção no estudo de Fase III
As mulheres com paridade geralmente relataram menos desconforto relacionado à inserção do que as mulheres nulíparas (p <0,0001 para a diferença geral).
No entanto, entre as mulheres nulíparas, 41,8% relataram não mais do que dor “leve” e 84,5% relataram não mais do que dor “moderada”.
4 Eficácia contraceptiva e retorno à fertilidade
Eficácia contraceptiva

Estudo de Fase III pivotal
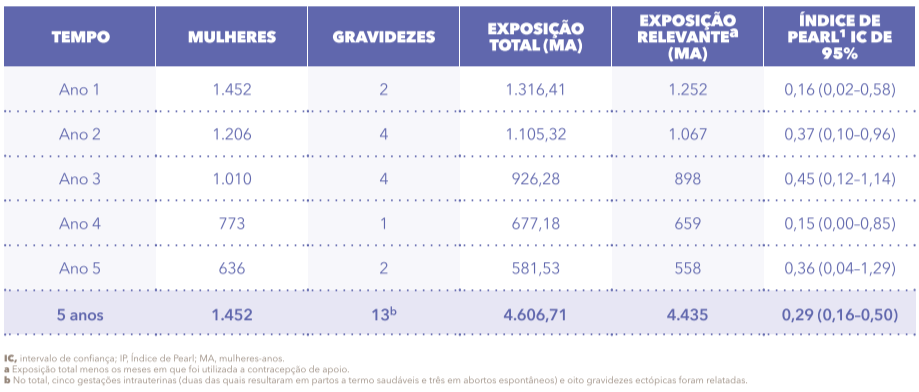
Kyleena® é altamente eficaz ao longo de 5 anos de uso.
• Índice de Pearl de 5 anos: 0,29
• Não houve declínio na eficácia ao longo do tempo
Retorno à fertilidade
O uso de Kyleena® não altera o curso da fertilidade futura. Quando o Kyleena® é removido, as mulheres retornam ao seu nível de fertilidade normal.
Mais de 70% das mulheres que interromperam o estudo devido a um desejo de gravidez conceberam nos primeiros 12 meses. Isso é consistente com os dados de retorno à fertilidade relatados após a descontinuação de outros SIUs.

No total, 179 mulheres descontinuaram o uso de Kyleena® devido ao desejo de engravidar. Das 163 mulheres sobre quem as informações de acompanhamento estavam disponíveis, 1,2% conceberam dentro de 12 meses.
5 – Segurança
Resumo do perfil de segurança
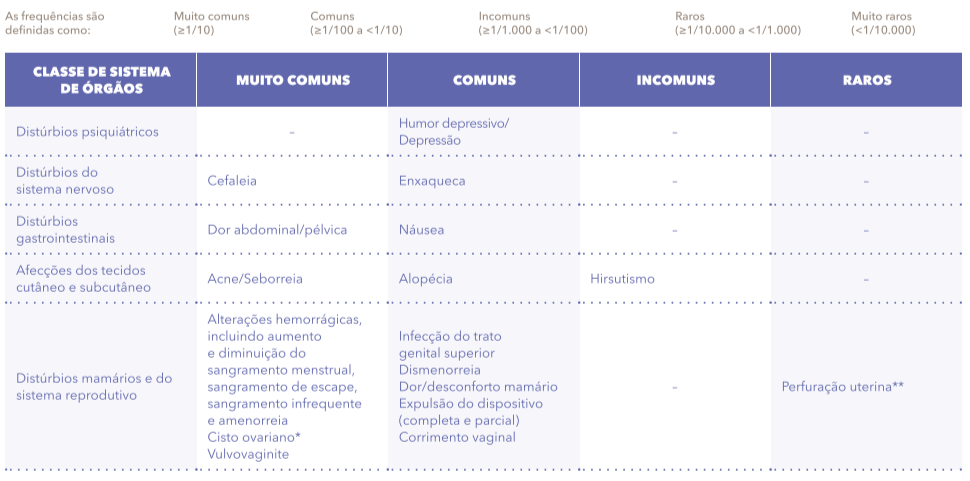
As frequências de reações adversas ao medicamento (RAMs) relatadas com Kyleena® estão resumidas na tabela abaixo. Dentro de cada grupo de frequência, os efeitos indesejáveis são apresentados por ordem decrescente de seriedade.
Gravidez ectópica
O uso de Kyleena® está associado a uma baixa taxa absoluta de gravidez ectópica (com base nos dados da Fase II e dos principais estudos de Fase III).
No entanto, se uma mulher engravidar enquanto estiver usando Kyleena®, há uma chance de aproximadamente 50% de que a gravidez seja ectópica.

As mulheres que consideram Kyleena® devem ser aconselhadas sobre os sinais, sintomas e riscos da gravidez ectópica.3 Fatores de risco conhecidos para gravidez ectópica incluem gravidez ectópica anterior, cirurgia tubária ou infecção pélvica. Estes fatores de risco aplicam-se independentemente do método de contracepção usado.2
No caso improvável de uma gravidez com Kyleena®, a possibilidade de gravidez ectópica deve ser considerada no caso de dor no baixo ventre, especialmente em conexão com menstruação não ocorrida ou se uma mulher amenorreica começar a sangrar.
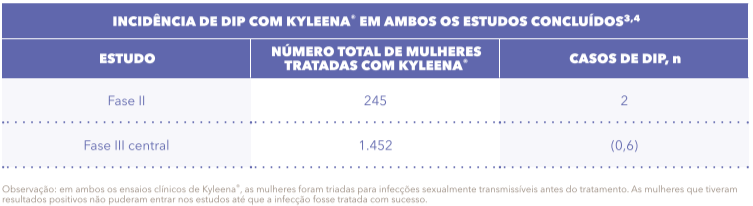
Doença inflamatória pélvica (DIP)
A frequência geral de DIP atribuível ao uso de contraceptivos intrauterinos parece ser baixa e concentrada nas primeiras semanas após a inserção. O risco subsequente de infecção é comparável ao de mulheres que não usam DIU de cobre e está fortemente associado a fatores de risco, como múltiplos parceiros sexuais, infecções sexualmente transmissíveis e histórico de DIP.
As infecções pélvicas, tais como a doença inflamatória pélvica, podem ter consequências graves e podem comprometer a fertilidade e aumentar o risco de gravidez ectópica.
A DIP ocorre quando micro-organismos sobem do trato genital inferior, infectando o útero, tubas uterinas e ovários. Chlamydia trachomatis e/ou Neisseria gonorrhea são frequentemente identificados entre mulheres com DIP. Embora o Kyleena® e o insertor, como tais, sejam estéreis, eles podem, devido a uma contaminação bacteriana durante a inserção, tornar-se um veículo de transporte microbiano no trato genital superior. Isso pode explicar um risco maior de DIP durante as primeiras semanas após a inserção de qualquer dispositivo intrauterino.
Perfuração uterina
Na Fase II e nos principais estudos de Fase III, Kyleena® foi associado a uma baixa taxa de perfuração uterina.

Perfuração ou penetração do colo ou corpo uterino por um contraceptivo intrauterino pode ocorrer, mais frequentemente durante a inserção, e pode diminuir a eficácia do Kyleena®. Tal sistema deve ser removido.
O risco de perfuração pode ser maior em mulheres com útero retrovertido fixo.
Além disso, a frequência de perfuração uterina foi avaliada em um grande estudo de coorte prospectivo, comparativo e não intervencionista em usuárias de Mirena® e de outros DIUs (N=61.448 mulheres). A incidência de perfuração foi de 1,3 (IC de 95%: 1,1-1,6) por 1.000 inserções em toda a coorte do estudo; 1,4 (IC de 95%: 1,1-1,8) por 1000 inserções na coorte do Mirena® e 1,1 (IC de 95%: 0,7-1,6) por 1.000 inserções na coorte de DIU de cobre.
O estudo mostrou que tanto a amamentação no momento da inserção como a inserção até 36 semanas após o parto estavam associadas a um maior risco de perfuração. Esses fatores de risco foram independentes do tipo de DIU inserido.
Expulsão
A taxa de expulsão do Kyleena® é baixa e na mesma faixa relatada para outros DIUs.

A expulsão do dispositivo em si é um evento não sério, mas a expulsão parcial ou completa de um SIU resultará em perda da eficácia contraceptiva. A expulsão pode estar associada a alguma dor ou sangramento, mas também pode passar despercebida (p. ex., durante um episódio de sangramento intenso). O uso do Kyleena® geralmente reduz a menstruação com o tempo; um aumento da menstruação pode, portanto, ser indicativo de expulsão.
Se o Kyleena® for parcialmente expelido (ou seja, presente no canal cervical), ele deverá ser removido. Um novo sistema pode ser colocado imediatamente, desde que a possibilidade de gravidez tenha sido excluída.
A mulher deve ser aconselhada a verificar os fios do Kyleena® e a entrar em contato com seu profissional de saúde se os fios não puderem ser sentidos.
6 – Padrão de Sangramento
A maioria das mulheres apresentam alterações no padrão de sangramento após a inserção de Kyleena®. Essas alterações são o resultado do efeito direto do LNG no endométrio e não refletem o ciclo ovariano.
Como a proliferação endometrial é inibida, pode haver um aumento inicial de escapes durante os primeiros meses de uso. Depois disso, a forte supressão do endométrio resulta em uma redução na duração e no volume do sangramento menstrual durante o uso de Kyleena® ao longo do tempo. Fluxo escasso se apresenta frequentemente como oligomenorreia ou amenorreia.
O número médio de dias/episódios de sangramento e sangramento de escape, de acordo com os critérios do padrão de sangramento da Organização Mundial da Saúde (OMS), foi analisado em cinco anos utilizando intervalos de referência (IR) de 90 dias.

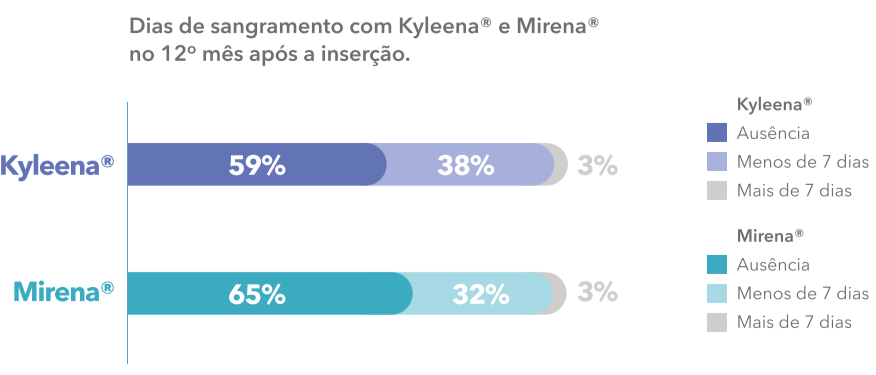
O padrão de sangramento de Kyleena® é similar ao de Mirena®. Kyleena® reduz progressivamente a intensidade e duração do sangramento.
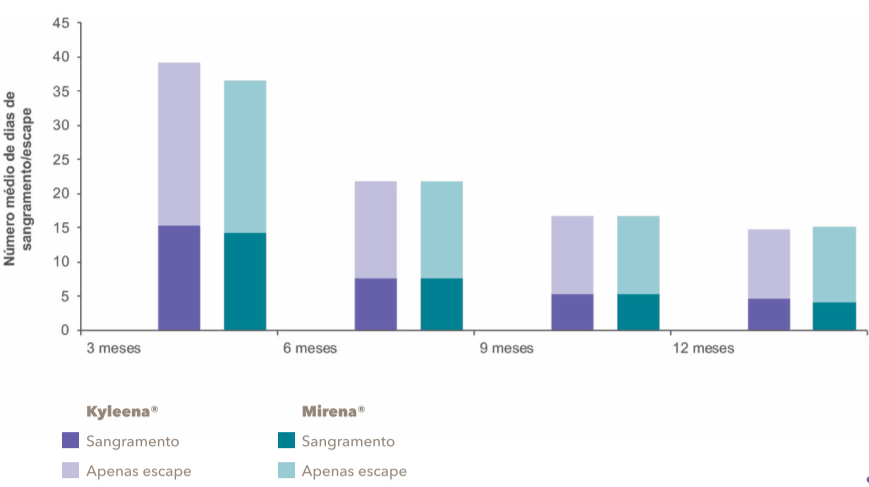
Kyleena® proporciona sangramento menos intenso e menos frequente.
59% das usuárias não apresentaram sangramento no 12º mês.
7 – Satisfação da usuária e descontinuação
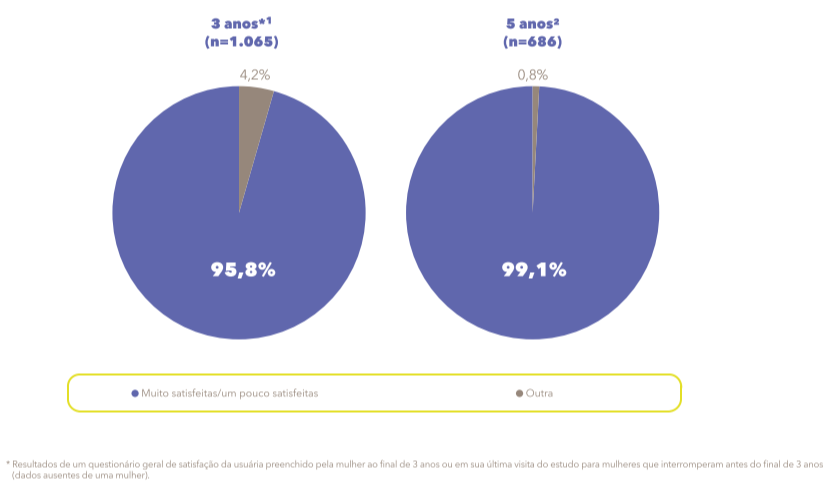
Kyleena® foi associado a altas taxas de satisfação da usuária1,2 Aos 3 e 5 anos, respectivamente:
• 96% e 99% das mulheres relataram que estavam “muito satisfeitas” ou “satisfeitas” com Kyleena®
Descontinuação
Estudo de Fase III pivotal: as principais razões para a descontinuação são típicas de mulheres em idade fértil que utilizam contracepção intrauterina.

Bula
Kyleena® – Levonorgestrel. Reg. MS-1.7056.0118. Indicações: Contracepção por até 5 anos. Contra-indicações: suspeita ou diagnóstico de gravidez; doença inflamatória pélvica atual ou recorrente ou condições associadas com aumento de susceptibilidade a infecções pélvicas; endometrite pós-parto; aborto infectado nos últimos 3 meses; vaginite ou cervicite aguda; neoplasia cervical; tumor maligno uterino ou cervical; tumores progestógeno – dependentes; sangramento uterino anormal não-diagnosticado; anomalia uterina congênita ou adquirida que podem interferir com a inserção ou retenção do SIU; doença hepática aguda ou tumor hepático; hipersensibilidade ao princípio ativo ou a qualquer um dos excipientes. Cuidados e advertências: enxaqueca focal com perda visual assimétrica ou outros sintomas indicativos de isquemia cerebral transitória; cefaleia excepcionalmente intensa; icterícia; aumento acentuado da pressão arterial; doença arterial grave, cardiopatia congênita ou valvulopatia. A glicemia deve ser controlada em pacientes diabéticas. Interações medicamentosas: indutores de enzimas microssomais, não se espera que seja de maior importância, considerando o mecanismo de ação local de Kyleena®. Eventos adversos: humor deprimido/ depressão, cefaleia, enxaqueca, dor abdominal/pélvica, náusea, acne/seborreia, hirsutismo, alopecia, alterações no padrão de sangramento, infecção do trato genital superior, cistos ovarianos, dismenorreia, mastalgia, perfuração uterina, expulsão, vulvovaginites. Posologia: Inserir uma unidade na cavidade uterina seguindo as regras de inserção. Cada administração é eficaz por 5 anos. VENDA SOB PRESCRIÇÃO MÉDICA. SAC 08007021241.
CONTRA INDICAÇÕES: SUSPEITA OU DIAGNÓSTICO DE GRAVIDEZ. INTERAÇÕES MEDICAMENTOSAS: INDUTORES DE ENZIMAS MICROSSOMAIS.
Material destinado exclusivamente à profissionais de saúde habilitados a prescrever medicamentos.